刚刚结束的ASCO年会期间,阿斯利康(AZ)再次大放异彩,连续第7年荣登全体大会报告舞台;自2020年以来已累计入选8项LBA研究,AZ在肺癌、乳腺癌等传统优势领域的统治力仍在延续,同时在消化道肿瘤新战场的影响力实现了现象级的跃升。未来如需更进一步,AZ无疑不想再错过细胞治疗这一推动未来增长的潜在催化剂,并期待从肿瘤和自免疾病两大领域双管齐下,倾力攀越新高度。
过去几年,AZ这家跨国制药巨头动作频频:2022年,收购Neogene布局TCR-T疗法;2023年“牵手”Quell布局治疗自免疾病的Treg疗法。而在CAR-T赛道,AZ通过收购亘喜生物拥有了下一代CAR-T疗法的关键筹码;同时也在与西比曼合作探索实体瘤CAR-T。今年,AZ又斥资10亿美元收购EsoBiotec,押注当下备受关注的体内细胞疗法。可以说,过去3年多,AZ在细胞疗法赛道的每一笔交易都别有巧思。
从研发进展而言,以CAR-T、TCR-T仍是当前全球制药研发的核心赛道。尤其是CAR-T疗法已在广泛血癌患者中带来了令人振奋的长期缓解,这无疑将会为癌症治疗的变革带来全新机遇。亘喜生物是AZ在CAR-T赛道的第一笔收购,这项重磅交易的核心是亘喜突出的技术与管线——FasTCAR和AZD0120。加入集团一年多后,AZD0120在近期再次高调亮相EHA和EULAR大会,亘喜同时发布了其针对NDMM和rSLE的多项数据,展现出强劲的临床开发动能,尤其是rSLE首次公布便入选EULAR口头报告,可见业界对其初步临床效果的认可度。
首发rSLE数据,入选口头报告
EULAR 2025年会期间,亘喜生物以口头报告首次公布了AZD0120治疗难治性系统性红斑狼疮(rSLE)的一项IIT研究的安全性及初步疗效数据。
入组10例患者,基线为既往经受过多重治疗的rSLE患者,SLEDAI-2K评分≥8,且均伴有狼疮性肾炎,中位随访时间达313.5天。总体而言,安全性和初步的临床效果都很积极。试验中未观察到DLT和ICANS,仅出现低级别CRS,这与此前在血癌领域观察到的结果基本一致,安全性优势在自免领域中的重要意义不言而喻;疗效层面,所有患者(100%)在完成单次输注后补体水平恢复正常。70%的患者实现ANA、ENA及dsDNA抗体持续血清学转阴,进入狼疮非活动期。截至2025年1月,90%的患者在第9个月达到DORIS标准缓解。所有患者(100%)蛋白尿显著减少,其中60%患者在第9个月达到KDIGO-2024 定义的完全缓解(CR),40%的患者达到部分缓解(PR)。
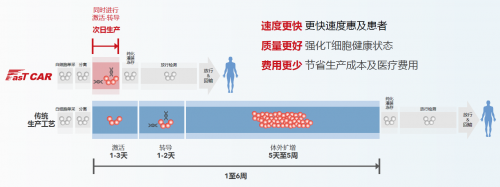
SLE是一种以致病性浆细胞、长寿命浆细胞和记忆B细胞产生自身抗体为特征,长期困扰患者生活,甚至危及生命的自身免疫性疾病。2023年的一项流行病学研究显示,全球有超340万人正饱受SLE的困扰,每年新确诊患者高达40万。由于SLE传统疗法疗效有限,副作用严重,且需长期用药,因此亟需更加安全、有效的药物打破SLE治疗僵局。AZD0120通过CD19/BCMA双靶点设计,结合次日生产技术,能更加深入、广泛地清除致病性B细胞和浆细胞,进而显著改善临床获益。从此次披露的初步数据来看,通过AZD0120治疗,使患者的致病性B细胞耗尽后,能再次诱导B细胞重新恢复为naïve B细胞,为最终实现患者“免疫系统重置”提供了巨大的机遇。这也有望让AZ除了已上市的阿伏利尤单抗后,能在未来进一步站稳广阔的SLE市场,想象空间巨大。
值得一提的是,去年底,CAR-T治疗自免疾病的突破性进展成功入选Science 2024年度十大科学突破,这是继2013年之后,时隔11年CAR-T技术再次入选,标志着该技术在自免领域的应用得到了重大认可。
更新NDMM数据,结果依旧振奋
在同期召开的EHA2025年会上,亘喜生物又接连发布了AZD0120作为新确诊多发性骨髓瘤(NDMM)一线疗法,分别针对符合移植条件的NDMM高危患者(TE NDMM)和不符合移植条件的NDMM老年患者(TI NDMM)的两项最新临床数据。两组都是更长随访时间下的更新数据,结果积极,让业界看到了该候选药物在NDMM早线治疗上的更多可能性。
就TE NDMM而言,截至2025年2月10日,中位随访时间为32.3个月。据称,这是迄今为止CAR-T治疗NDMM患者最长的前瞻性随访。疗效方面,ORR保持100%, sCR率为95.5%,且所有患者(100%)均达到MRD阴性,30个月PFS率为85.7%。安全性数据与早期结果高度一致,只有少量患者出现CRS。
这些数据与前一次的更新数据研究结果一致,AZD0120在TE HR NDMM 患者中诱导了深度、持久的缓解,且具有非常有利的安全性优势,突出了AZD0120治疗高危 NDMM患者的潜力,并为此前预后不佳的患者带来了新希望。
而在TI NDMM方面,亘喜还公布了另一项针对老年患者的疗效及安全性。一般而言,70岁以上的MM患者通常会因身体限制而无法移植,且难以入组。这项研究招募了9例患者,中位年龄为72岁(范围70-78)。截至2025年2月10日数据截止,中位随访时间为13.9个月。 研究显示,AZD0120治疗后,患者ORR及sCR率均为100%。所有患者(100%)均达MRD阴性,且截至数据截止日,均未观察到疾病进展。安全性方面,50%患者经历了1级CRS,所有患者在5天内从CRS中恢复。未观察到≥2级CRS及任何级别的ICANS。
这些数据也在作证,AZD0120在老年MM患者中同样表现出令人振奋的临床疗效及安全性,有望为70+ TI NDMM患者带来全新的治疗选择。该试验带来的非常重要的启示是,或许实足年龄不应作为CAR-T细胞临床试验排除患者的标准或在真实世界中排除患者接受BCMA CAR-T治疗的标准,这对于填补临床治疗领域空白意义重大。
MM是世界上第二常见的血液系统恶性肿瘤。到2028年,MM药物主要市场销售额预计将达437亿美元,2033年将达521亿美元。鉴于当前CAR-T疗法这该领域中“呼风唤雨”的获益,谁能尽快占领NDMM赛道,势必能分到最大份额的“蛋糕”。尽管MM领域已有4款CAR-T获批上市,但目前尚未有产品获批一线治疗。如果AZD0120能够把握一线治疗机遇,背靠AZ的商业化能力,将有很大希望冲击重磅炸弹药物俱乐部。结合在自免领域的最新表现,目前来说,AZD0120是AZ细胞疗法矩阵中当之无愧的“关键牌”。在今年多次对外公开展示中,AZ均将其作为驱动2030+增长的重点期待品种。
回首2023年12月,AZ以12亿美元收购亘喜生物的开创性交易,不仅创造了中国Biotech史上前所未有的发展路径,同时也是AZ“in China-For Global”战略的一次重要实践。值得注意的是,AZ曾明确提及,未来将以上海作为细胞治疗领域的重要研发基地,借助中国这一创新策源地,进一步推动细胞治疗的发展。作为AZ细胞疗法版图中的“中国创新力量”,随着融合的深入,亘喜生物的开创性技术与跨国药企的全球平台如何相得益彰,进一步孕育AZ新的“拳头产品”,将是双方重磅交易未来的看点。
免责声明:本文是转载企业宣传资讯,仅代表作者个人或企业观点,不代表本站立场。内容仅供参考,并请自行核实相关内容。
